01
《行动计划》工作任务中明确要强化药品器械管理。医疗机构依法依规确定本机构药品器械供应目录,加强重点监控合理用药药品、抗微生物药物、抗肿瘤药物以及放射影像设备、植入类器械等常用设备器械的管理,做好药品器械不良反应的监测报告,对不良反应多且安全隐患突出的药品器械要及时依法依规清退出供应目录。
近年来,国家对于医疗器械不良反应的重视程度逐步加深。根据国家药品不良反应监测中心发布的《国家医疗器械不良事件监测年度报告(2022年)》,2022年国家医疗器械不良事件监测信息系统共收到医疗器械不良事件报告694,866份,比上年增加6.79%。
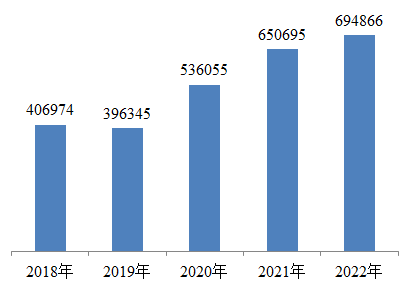
2018-2022年全国医疗器械不良事件报告数量
其中,涉及Ⅲ类医疗器械的报告244,154份,占报告总数的35.14%;涉及Ⅱ类医疗器械的报告329,732份,占报告总数的47.45%;涉及Ⅰ类医疗器械的报告58,057份,占报告总数的8.36%;未填写医疗器械管理类别的报告62,923份,占报告总数的9.06%。
从最近文件可以看出,未来医疗机构对于医疗器械不良反应的监控将更为严格,这将倒逼企业从研发到生产环节全面升级,以免被清退出供应目录。
02
《行动计划》提到要:规范医疗技术管理。医疗机构全面梳理本机构医疗技术临床应用情况,以限制类技术、内镜和介入技术等为重点加强质量安全管理,强化新技术、新项目机构内准入管理,完善技术授权和动态管理等相应的管理制度及工作流程,在保障医疗质量安全的基础上,加强新技术临床应用和适宜技术推广。
随着《医疗器械监督管理条例》、《医疗器械注册管理办法》、《医疗器械临床试验机构条件和备案管理办法》等文件的不断修订,针对临床上医疗器械的选择和使用的态度愈发严格,然而这并非是在限制新技术、新项目进院,而是为了确保临床使用的安全性和有效性,避免出现“劣币驱逐良币”的情况。
此前发布的《创新医疗器械特别审批程序(试行)》和《医疗器械优先审批程序》,对于鼓励医疗器械产业创新,促进临床急需的医疗器械尽快上市发挥了重要作用。符合条件的相关医疗器械可以申请按相应程序加快审批。
今年3月,国家医保局公开《对十三届全国人大五次会议第3298号建议的答复》(以下简称《答复》),其中对新技术、器械、高值耗材等的付费方式做出答复,
03
《行动计划》提出,提高检查检验质量。要建立健全覆盖检查、检验全过程的质量管理制度,加强室内质量控制,重点关注即时检验(POCT)质量管理,配合做好室间质量评价工作,充分发挥质量管理对于推进医疗机构检查检验结果互认的重要作用。进一步优化危急值项目管理目录和识别机制,强化危急值报告的及时性、准确性。
POCT具备方便、快捷、高效率、低成本等优点,市场前景广阔,行业增速快。据统计,近几年市场复合增速高达 26%。2021年,IVD全球市场份额1170亿美元,POCT市场规模占比29%,位居各细分市场第一。
同时,国内POCT市场也保持着高速增长。据统计,2021年我国POCT行业市场规模达111.6亿元,预测2025年我国POCT行业市场规模将达到231.4亿元。
此次文件着重强调关注POCT,该赛道相关企业有望实现高速发展。
04
《行动计划》指出要提高急难危重救治效果。
医疗机构进一步优化绿色通道管理,做好急难危重患者分类,完善抢救资源配置与紧急调配机制,保障各单元抢救设备和药品可用,确保急危重患者优先救治,加强危急值处置管理,提高危急值处置的及时性、规范性。进一步落实急危重患者抢救制度和疑难病例讨论制度,提高重症患者救治技术能力。
今年发布的《2023三级公立医院绩效考核操作手册》,在日间手术择期手术比例、出院患者手术占比、出院患者微创手术占比、出院患者四级手术比例等方面都进行了修订,从考核层面对手术质量安全提出了更高要求。
此外,《行动计划》还提出,医疗机构要进一步强化“以患者为中心,以疾病为链条”的理念,打破传统学科划分和专业设置壁垒,以多学科协作(MDT)为基础,探索专病中心建设,为患者提供重大疾病诊疗一站式服务。
对于医疗机构而言,多学科协作模式能够在多科室之间形成合力,进而提高临床诊疗效率。与此同时,医疗器械临床试验是一个多学科协作、系统性的工作。当传统壁垒被打破,医疗器械从研发到销售都会实现长足发展。
《行动计划》发布,未来3年医疗质量领域大方向已定。国家始终围绕着提高医疗服务质量的目的,促进公立医院发展,而与其密切相关的医疗器械市场即将迎来新的机遇和挑战。