过去20年,中国医疗器械行业以“模仿式创新”打破海外垄断,快速缩短与发达国家的差距。尤其是低值医用耗材和中低端医疗设备领域,国产企业已在全球市场占据一定优势。
如今,中国医疗器械市场已成为全球第二大市场,2025年市场规模将突破1万亿元。在这个规模超万亿元的市场,“模仿式创新”显然不再能满足需求。因此,中国医疗器械行业需要从“模仿式创新”转向“基于临床需求的原始创新”。
不过,对于投资人而言,“基于临床需求的原始创新”通常具有高技术门槛和壁垒,且具有研发周期长、前期投入大、不确定性高、风险大等特点。但是,“基于临床需求的原始创新”却有望颠覆原有市场格局,带来新一轮产业革命。
一边是巨大风险,一边是巨大收益。对此,越来越多的投资人选择拿出真金白银“投早、投小”,以推动科技创新、加速产业变革。目前,这些投资人手握大把钞票,正在寻找下一个医疗器械颠覆性创新技术。
动脉网通过与数位投资人沟通交流,并根据以往投融资数据及创新技术的发展阶段,找到了5个创新性强、商业化潜力大、有望颠覆现有市场的创新技术,供大家参考。
一、介入式人工心脏(pVAD)
介入式人工心脏(pVAD),即经皮置入心室辅助装置,是将小型血泵经皮以介入方式置入心室,通过血泵的作用引流血液进入动脉系统,实现部分或全部替代心脏泵血功能,起到维持人体血液循环的作用。
介入式人工心脏可应用于急性心肌梗死救治、高危PCI手术防护等临床场景,有助于提高相关适应症的抢救存活率。其中,急性心肌梗死救治、PCI等手术,我国每年开展超百万例,市场空间巨大。
在海外,Abiomed已验证了介入式人工心脏的临床价值及商业价值。从临床上看,Abiomed推出的介入式人工心脏产品Impella系列已在全球应用,并已被多个临床指南推荐应用。不过,该产品的渗透率仍处较低水平,还有极大发展空间。
从商业上看,2022财年,Abiomed营收10.3亿美元,同比增长22%,其中来自介入式人工心脏产品的收入为9.85亿美元,占比超95%。可以说,Abiomed靠介入式人工心脏产品撑起了166亿美元估值(约合人民币1150亿)。2022年11月,强生宣布以166亿美元收购Abiomed,同时,若未来达成既定商业和临床试验里程碑,Abiomed的股东还将额外获得最高每股35美元现金权益。
全球范围内,目前仅Abiomed的Impella系列获FDA批准,国内则尚无任何一款介入式人工心脏产品获批。不过,国内已有通灵仿生、心岭迈德、心擎医疗、迪远医疗、丰凯利医疗、心恒睿医疗、核心医疗等企业布局,还有红杉中国、君联资本、鼎晖VGC、千骥资本、雅惠投资、泰福资本、元生创投、辰德资本、礼来亚洲基金、正心谷资本等知名投资机构押注。
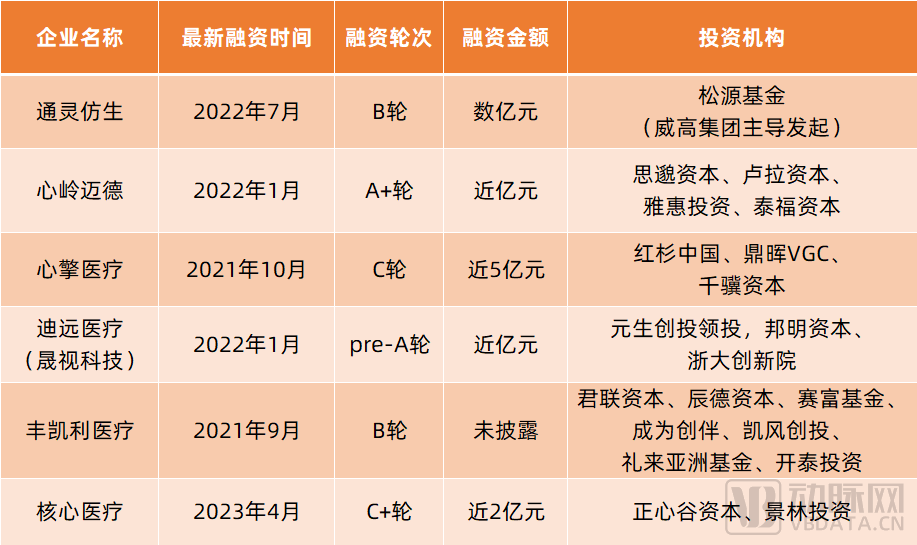
其中,通灵仿生已完成动物实验、型式检验,即将进入临床试验;心岭迈德、心擎医疗、迪远医疗、核心医疗均已开展动物实验;丰凯利医疗自主研发的的SynFlow®3.0已于2023年1月进入NMPA创新医疗器械特别审查程序。
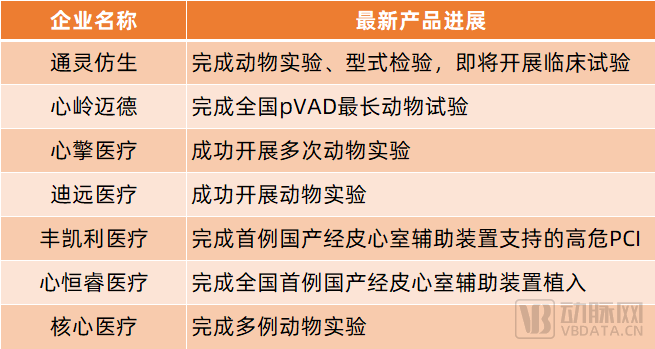
根据公开信息整理
二、组织工程小口径人工血管
当人体血管由于疾病、创伤等因素不能正常运输血液时,人工血管可置换血管或旁路搭桥,使血液能够正常运输。目前,人工血管被广泛应用于主动脉置换或搭桥、外周血管旁路移植术、血管创伤修复、血液透析血管通路、冠脉旁路移植术等多种临床场景。
根据《全球及中国人造血管行业研究及十四五规划分析报告》,2020年全球人工血管市场规模达到235亿元,预计2027年将达到318亿元。
按照口径大小,人工血管被分为大、中、小三种规格,通常称10毫米以上的为大口径人工血管,介于6毫米和10毫米之间的为中等口径,小于6毫米的是小口径。其中,如今临床上应用的主要为大、中口径人工血管,全球仍未有小口径人工血管获批。
与此相对的是,小口径动脉疾病具有较高的发病率和死亡率。若开发出小口径人工血管,不仅能救治更多血管病患者,还可极大开拓人工血管市场,并取得丰厚商业回报。
据介绍,大、中口径人工血管主要以涤纶和膨体聚四氟乙烯为主要材料。此种材料制造小口径人工血管时存在血栓、内膜增生、感染等问题,临床表现不佳。不过,随着材料科学的突破及组织工程技术的发展,已有多家创新企业研发布局小口径人工血管,并已取得优异临床数据。
业内人士认为:随着依靠新材料、新技术的人工血管公司崛起,传统的不可吸收高分子人工血管将退出历史舞台。
例如,人工血管领先企业Humacyte研发的人类脱细胞组织工程血管(HAV),采用组织工程技术,在人体外生成“活”的人体血管,临床表现优异。截至2021年底,HAV已植入约471名患者体内,迄今为止没有免疫排斥反应。Humacyte估计,若HAV产品最终获得FDA批准,其血管产品的潜在峰值销售额每年将达到121亿美元。
值得一提的是,2018年,费森尤斯就与Humacyte的HAV技术商业化权利签署了1.5亿美元的战略合作协议。
在国内,领博生物、柔脉医疗、武汉杨森、海迈医疗等创新企业也已依托组织工程等技术布局小口径人工血管。
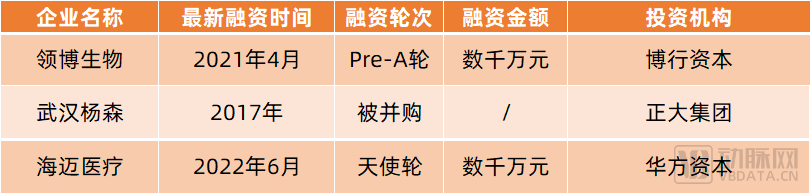
其中,领博生物自主研发的生物型人工血管已于2022年8月完成首例临床入组;柔脉医疗已研发出小口径组织工程化人工血管与组织化电子血管;武汉杨森研发的小口径人工血管已获批进入绿色通道,并进入动物实验阶段;海迈医疗研发出了自体和同种异体脱细胞基质小口径人工血管。

根据公开信息整理
三、高分子瓣膜
高分子瓣膜是一种基于新材料和新技术、能够更好治疗心脏瓣膜病的创新器械。
《中国心血管健康与疾病报告2021》显示,中国约有2500万例瓣膜性心脏病患者,在中国65岁以上人群中,心脏瓣膜疾病越来越普遍。预计随着人口老龄化趋势的增加,瓣膜疾病的发病率将逐年上升。
从临床上看,心脏有二尖瓣、三尖瓣、主动脉瓣和肺动脉瓣四个瓣膜。其中,预计2030年二尖瓣介入治疗市场规模将达1200亿元;主动脉瓣介入治疗市场规模将达1100亿元……市场空间极为广阔。
在治疗上,针对严重瓣膜性心脏病患者,更换人工心脏瓣膜是最有效的治疗手段。据介绍,目前临床上常用的人工心脏瓣膜依据材料可分为机械瓣(以热解碳制作)和生物瓣(以猪、牛等来源的生物组织制作)。
机械瓣的优势是使用时间长,设计使用寿命超过50年,但热解碳材料的血液相容性差,易引发血栓栓塞等并发症,且患者术后必须终生服用抗凝药物,极大影响患者的生活质量。
生物瓣的优势则是以生物组织制作,具有较好的血液相容性,只需在术后3-6个月服用抗凝药。不过,生物瓣的使用寿命仅有10-15年,难以满足目前越来越年轻的瓣膜病患者的需求,甚至部分患者在瓣膜置换不久后就出现瓣膜组织钙化,并引起瓣膜衰败。
随着材料科学的突破,有创新企业研发出融合了机械瓣及生物瓣双重优势的高分子瓣膜。与传统机械瓣和生物瓣相比,高分子瓣膜具有优异的耐疲劳性,使用寿命长,且具有极好的血液相容性,患者无需长期服用抗凝药。
例如,全球高分子瓣膜领域先驱企业Foldax推出的高分子瓣膜产品已进入人体临床试验阶段。现有临床数据表明:Foldax的高分子瓣膜产品比传统生物瓣膜的使用寿命更长,长达25年;高分子瓣膜植入一年后,患者的跨瓣压差、瓣膜有效开口面积(EOA)和心功能均得到了明显改善,且患者无需长期服用抗凝药。
目前,全球范围内仅有少数企业掌握高分子瓣膜技术。其中,国内有心岭迈德、心锐医疗、以心医疗等企业布局。
截止目前,心岭迈德已完成首例国产高分子外科瓣膜动物实验;心锐医疗同步研发了高分子外科主动脉瓣、二尖瓣以及介入主动脉瓣;以心医疗自主研发的高分子经股主动脉瓣置换系统已于2022年7月完成首例临床。

根据公开信息整理
四、脉冲电场消融技术
脉冲电场消融技术是一种基于不可逆电穿孔效应的创新消融方式,目前正被探索性应用于房颤消融,被称为PFA(脉冲电场消融系统)。其中,不可逆电穿孔是指在一定的电场强度下,细胞膜永久通透,细胞内容物泄露,致使细胞凋亡。
研究表明:脉冲电场消融技术具有组织选择性。例如,在针对心肌细胞的特定电场参数下,心肌细胞会发生不可逆电穿孔,而内皮细胞、神经细胞、平滑肌等不受影响。
目前,关于房颤的消融治疗主要以射频消融与冷冻消融为主。射频消融技术是通过射频电流使病变组织产生热效应,消融心肌细胞,从而治疗房颤;冷冻消融技术是通过制冷剂的蒸发吸热效应,使病变部位温度骤然降低,并使病变区域细胞受损或死亡,从而治疗房颤。
与射频消融及冷冻消融治疗房颤的原理一致,脉冲电场消融也是通过“杀死”对应的病变细胞,从而恢复心房正常有序的电活动。
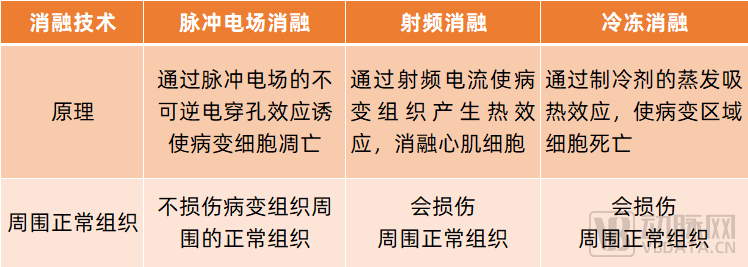
不过,射频消融与冷冻消融利用温度效应消融细胞,易造成病变部位周围正常组织受损,引发并发症。而脉冲电场消融技术基于组织选择性,可有选择性地杀伤心肌组织,确保膈神经、神经、冠脉等其他正常组织的安全,从而提高治疗效果,降低术后并发症。
事实上,脉冲电场消融技术还可应用于多种临床场景,如肿瘤消融。相比于肿瘤消融中常见的射频消融和冷冻消融方式,脉冲电场消融可选择性消融肿瘤组织,保存治疗区内的动脉、胆管、神经束、支气管等重要结构,并可治疗其他设备无法消融的肿瘤,如血管、神经周围的肿瘤。
从市场看,我国心脏电生理市场规模预计到2023年将达到123.2亿元,肿瘤消融行业市场规模预计到2023年将达到61.5亿元。而脉冲电场消融技术较射频消融、冷冻消融具有原理性优势,有望成为未来的主流消融技术。
或许也是因此,波科、强生、美敦力等跨国械企均已开始布局相关产品管线。在国内,惠泰医疗、捍宇医疗、微电生理、锦江电子、睿笛生物、德诺电生理、玄宇医疗、艾科脉、洲瓴医疗、睿刀医疗、迈微医疗、远山医疗等企业也已有所布局,且进展极快。
其中,睿笛生物的纳秒脉冲肿瘤消融系统已完成全部临床入组,心脏房颤脉冲电场消融系统已进入临床试验;锦江电子的脉冲电场消融系统于2021年11月完成注册临床试验的全部病例入组;惠泰医疗的心脏脉冲消融PFA系统于2023年2月完成上市前临床试验的全部患者入选……总的来看,预计国产脉冲电场消融系统将快速陆续获批。
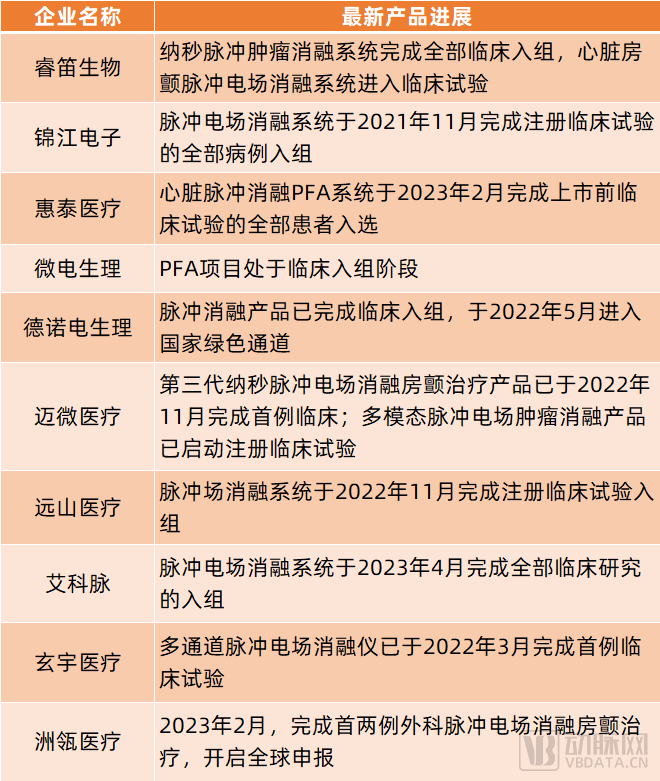
根据公开信息整理
五、血管内冲击波技术
血管内冲击波技术是美国上市公司Shockwave受超声波碎石技术启发而创新出的一种适用于血管内钙化的新技术。同时,Shockwave还基于血管内冲击波技术研发出了用于冠脉及外周血管钙化的冲击波球囊。
目前,Shockwave市值约为106亿美元(约合人民币735亿元)。5月11日,有媒体报道:强生及美敦力考虑联手收购医疗公司Shockwave。此前,有媒体于4月曝出波士顿科学正探索收购Shockwave。无论消息真假,可见市场对血管内冲击波技术的关注度极高。
而血管内冲击波技术针对的中重度血管钙化也行业长期存在的难题,其不仅有可能导致血管成形术失败,还会增大手术风险、增加手术即刻并发症及支架内血栓的发生率。另一方面,血管钙化是动脉粥样硬化、高血压、糖尿病血管病变、血管损伤、慢性肾病等普遍存在的共同病理表现,具有发病率高、危害大的特点。
基于庞大患者数及严重疾病危害,冲击波球囊或将成为血管钙化患者的刚需。
此前,市场上也有多种解决方案,如斑块旋磨术(RA)、准分子激光冠脉斑块消蚀术(ELCA)、冠脉轨道旋磨术(OAS)。但是,此类治疗方式均有一定局限性。
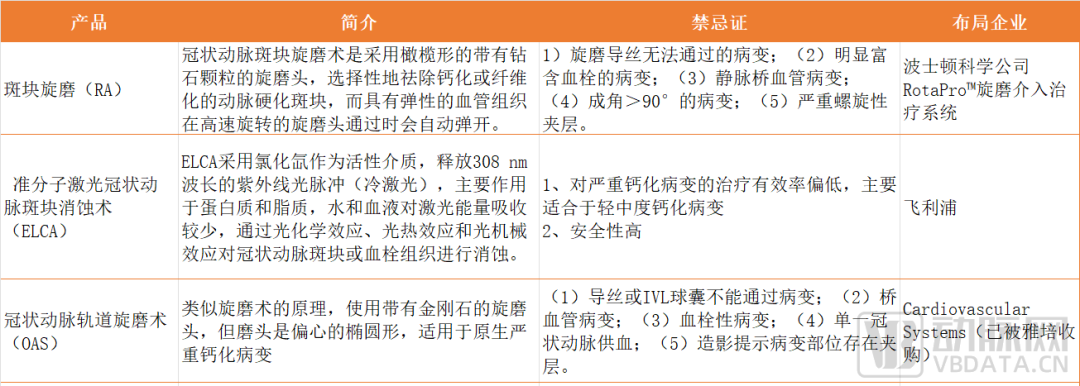
相比于传统治疗方案,冲击波球囊在植入病变血管段后,可释放脉冲声压波,将钙化斑块“震松”,最终轻松植入支架等治疗器械,使患者血流重建、心脏功能恢复正常。
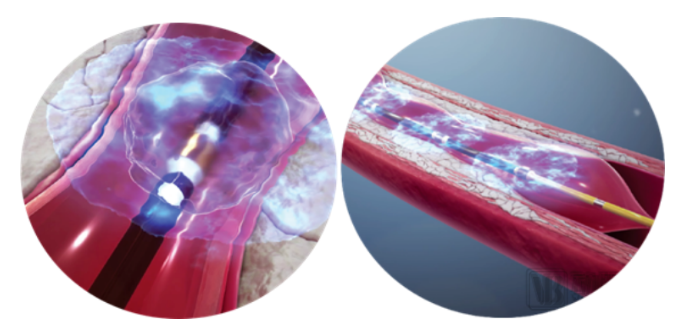
Shockwave的产品作用于血管示意图
在治疗效果上,Shockwave发布的临床试验数据显示,冲击波球囊在血管钙化病变的治疗中,安全性高、心血管主要不良事件发生率低,无穿孔、远端栓塞、急性闭塞等严重并发症;有效性好,手术成功率高、术后管腔即刻获得高、管腔残余狭窄率低、支架扩张良好。
如今,健适医疗与Shockwave合作,已将其冲击波球囊引进国内,并于2022年获NMPA批准。除了健适医疗,国内还有谱创医疗、中荟医疗(汇禾医疗子公司)、赛禾医疗、乐普医疗、蓝帆医疗、北芯医疗等多家企业布局血管内冲击波技术。
其中,谱创医疗自主研发的外周冲击波球囊和冠脉冲击波球囊均已于2021年开展注册临床试验;中荟医疗研发的震波导管系统已于2021年进入确证性注册临床研究;赛禾医疗研发的冠状动脉和外周动脉血管内冲击波碎石系统已于2022年进入临床试验;乐普医疗研发的脉冲声波球囊系统已于2022年2月完成首例腘动脉严重钙化病变开通手术;蓝帆医疗旗下的冠状动脉血管内碎石系统已于2023年2月完成首例临床入组……
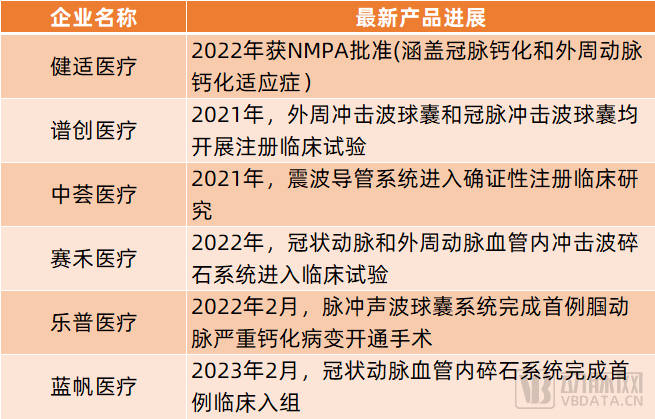
根据公开信息整理
除此外,沛嘉医疗还研发出冲击波瓣膜治疗系统,将血管内冲击波技术拓展应用于心脏瓣膜钙化性狭窄的治疗。目前,沛嘉医疗的冲击波瓣膜治疗系统已完成多例手术,均展现出良好的安全性及治疗效果。
