分子诊断市场主要划分为感染检测板块、肿瘤检测板块、生育健康和遗传病板块等。受新冠病毒检测需求的驱动,近年的体外诊断市场尤其是分子诊断市场迎来了爆发性增长。
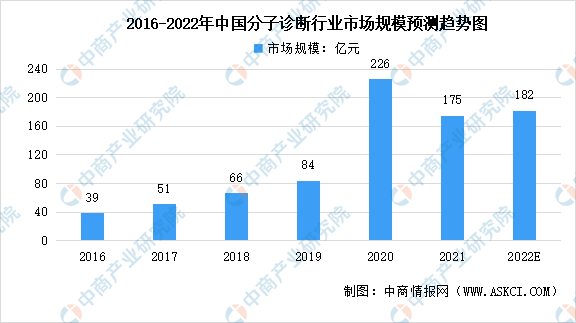
数据显示,中国分子诊断行业市场规模由2016年的39亿元增长至2019年的84亿元,年均复合增长率达28.9%。由于2020年新冠疫情的爆发,分子诊断市场规模迅速扩大至226亿元。中商产业研究院预测,2022年中国分子诊断行业市场规模将达182亿元,虽然比2020年的高位有所下降,但仍显示高速发展的态势。
分子诊断是临床上检测微生物病原体的一种重要手段,包括细菌、病毒、真菌、寄生虫、支原体等常见病原体的检测。 分子诊断也是预测诊断的主要方法,既可以进行个体遗传病的诊断,也可以进行孕妇的产前诊断。分子诊断的靶标主要是病原体或人体编码的各种结构蛋白、酶、抗原抗体等分子的独特基因序列。
分子诊断产业的上游为各类生物化学原材料、实验耗材、生产设备和包装材料等。由于历史原因,我国分子诊断试剂上游原料主要依赖进口,导致制造成本高昂。随着我国越来越多的企业掌握了原料的核心制备技术,国产体外诊断试剂原料的占比也不断走高。 2015年国产试剂原料的占比只有9.1%,至2020年国产占比已经接近12%,预计在2024年,国产试剂原料占比能够提高至13.5%。同时,分子诊断上游产业原料的价格也将会随着国产化的推进而逐步得到降低。 分子诊断产业的中游为使用基本原料制成的分子诊断试剂。目前我国分子诊断行业的市场规模不断扩大,分子诊断市场规模从2016年的39亿元人民币上涨至2021年的175亿元。 分子诊断相关技术的发展也相当迅猛,荧光定量PCR、基因测序、RNA恒温扩增法、FISH等多项分子诊断应用技术得到了蓬勃的发展。2021年中国PCR技术与基因测序技术专利申请数量为7648项,虽较2020年高峰期有所下滑,但技术发展势头仍然相当猛烈。 毫无疑问,分子诊断技术在过去一二十年丰厚的技术积累,加上疫情期间海量检测需求的驱动,疫情后各条产线常规分子检测项目的蓬勃开展,将使得分子产业的中游持续高速发展。 目前感染检测板块是分子诊断最大的单一细分市场,主要包括血液传染病、呼吸系统感染疾病等领域。其中血液传染病主要包括人类免疫缺陷病毒(HIV)、乙型肝炎病毒(HBV)、丙型肝炎病毒(HCV)等。 国内血液传染病分子诊断市场从2015年的10.07亿元增长到2020年的26.46亿元。伴随着我国对血液染病的重视程度加深,血液传染病分子诊断市场将逐步增长。预计2024年血液传染病分子诊断市场规模将在57.6亿左右。 呼吸道病原体主要包括结核分枝杆菌、新型冠状肺炎病毒、甲型流感病毒、肺炎支原体等领域。2020年国内呼吸道感染分子诊断市场由于新冠肺炎的爆发而高速增长,市场规模为140.27亿元。预计2024年,新冠疫情得到控制后,呼吸道感染分子诊断市场规模将保持在27亿元左右。
传统的病原体核酸检测流程步骤繁琐,耗时长,从样本采集、标本转运、核酸提取、核酸检测到最终出具报告往往需要6-10个小时。并且,传统的病原体尤其是病毒的检测模式对场所、环境、操作人员有着很高的要求,设备场地和人力的投入巨大,难以满足急诊、发热门诊管理、基层医疗机构、出入境、食品检测等场景的快速、简便检测需求。因此自动化核酸检测设备应运而生。 随着我国开展了多场全民核酸检测行动以及核酸检测常态化,大规模核酸检测成为刚需,推动基层核酸检测市场兴起,传统需要手工操作、提取效率低的设备显然无法满足要求。 由于我国基层医疗机构分子检测能力不足,卫健委在2020年4月、6月、7月多次发布政策,要求加强实验室建设;9月,国务院联防联控机制印发《进一步推进新冠病毒核酸检测能力建设工作方案》,强调“到2020年9月底前,实现辖区内三级综合医院、传染病专科医院、各级疾控机构以及县域内至少1家县级医院具备核酸采样和检测能力。” 通过这两年坚持不懈的努力,目前几乎所有二级综合医院都具备了核酸采样和检测能力,各地均已完成了城市检测基地和公共检测实验室建设。这些在新冠疫情下建立起来的较完善先进的核酸检测硬件和软件,在疫情后将为其他领域各种分子诊断包括肝炎、血筛、呼吸道、妇幼、癌症早筛等项目的开展奠定良好的基础,必将促进诊断产业持续高速发展,更好地服务于人民健康,更好地促进我国精准医疗事业的发展。 毫无疑问,对于产品线单一、只靠“新冠”的企业来说,随着新冠病毒检测市场的退潮,这类企业有可能被淘汰。而对于有着完善产品线和深厚市场布局的企业来说,新冠疫情后,各项常规及创新产品将回归正常增长。 据统计,目前国内的体外诊断企业已经超过1500家,市场竞争日益激烈,某些细分赛道已经非常拥挤,造成低价竞争状态。同时,随着体外诊断集采的逐步实行,国内IVD市场的利润空间进一步受到压缩。因此,许多企业瞄准了海外市场,布局海外市场目前已成为国内许多IVD公司的共识。

圣湘生物全力打造精品工程,研发了传染病防控、癌症防控、妇幼健康、血液筛查、突发疫情防控、慢病管理等一系列性能赶超国内外先进水平的分子检测产品,形成了集试剂、仪器、测序服务、第三方医学检验服务、分子实验室共建等为一体的全产业链系统解决方案,产品远销多个国家与地区。 未来,圣湘生物也将一如既往地为人民大众提供用得起、用得好的分子诊断产品和服务,为提升国民健康水平而贡献力量。